Als Hauptrisikofaktor für die Entstehung von Blasenkrebs gilt das Rauchen, wobei wie beim Lungenkrebs das Erkrankungsrisiko mit der Anzahl der gerauchten Zigaretten steigt und mit dem Zeitintervall nach Beendigung des Rauchens wieder sinkt.
Ca. 20 % aller Blasentumore sind auf berufsbedingte Umwelteinflüsse zurückzuführen, wobei insbesondere eine langjährige Exposition (bis zu 30 – 50 Jahre) mit Kanzerogenen (krebserregenden Stoffen), v.a. Bezidinderivaten, Aldehyden, chlorierten aliphatischen Kohlenwasserstoffen , aromatischen Aminen die Ursache ist. Daher ist Blasenkrebs als Berufskrankheit – v.a. bei Exposition mit aromatischen Aminen – bei zahlreichen Berufen wie z.B. Arbeiter in der Farbstoffchemie-, Leder- und Stahlindustrie, Maler, Automechaniker , LKW-Fahrer,Friseure, Zahntechniker anerkannt. Nach einer Strahlentherapie im kleinen Becken kann mit einer langjährigen Latenzzeit ein Harnblasenkarzinom v.a. bei älteren Patienten auftreten. In wissenschaftlichen Studien konnte eine Zusammenhang von chronischen Harnwegsinfektionen und einem erhöhten Erkrankungsrisiko an Harnblasenkrebs festgestellt werden. In sehr seltenen Fällen kann die Tropenkrankheit Blasenbilharziose eine Sonderform des Blasenkrebses (Plattenepithelkarzinom) auslösen. Am häufigsten gehen Blasentumore vom Urothel (Schleimhaut) der Harnblase, Harnleiter und der Nieren aus (Urothelkarzinome) und man findet sie oft multilokulär an mehreren Stellen. Seltenere und aggressivere Blasentumore sind die Plattenepithel- und Adenokarzinome der Harnblase. Der Blasenkrebs zeigt auch unterschiedliche Wachstumsformen : flache Tumore (carcinoma in situ), papilläre (warzenartige) und solide Tumore.
Als oberflächliche Blasentumore (Cis, Ta-T1) werden die Karzinome bezeichnet, deren Wachstum sich auf die innere Schleimhaut der Blasenwand beschränkt und noch nicht tiefer in die Blasenwand eingedrungen sind. Sie wachsen fingerförmig, polypartig in die Blase oder breiten sich sehr oberflächlich aus. Ist der Blasentumor allerdings auch in das Muskelgewebe eingedrungen, liegt ein muskelinfiltrierendes Karzinom (T2) vor.
-
Symptome
Das häufigste Symptom des Blasenkarzinoms ist die Hämaturie (Blut im Urin) . Patienten entdecken oft selbst mit dem Auge Blut im Urin (Makrohämaturie) oder der Arzt stellt bei einer mikroskopischen Urinuntersuchung zufällig rote Blutkörperchen fest (Mikrohämaturie). Dabei müssen nicht unbedingt Schmerzen auftreten.
Daher ist zunächst jedes schmerzlose Auftreten von Blut im Urin tumorverdächtig, solange keine andere Ursache dafür gefunden werden kann.
Eine urologische Untersuchung ist in diesem Fall sofort notwendig!Umgekehrt können die Beschwerden einer harmlosen akuten Blasenentzündung gleichen (Brennen beim Wasserlassen, Harndrang, häufiges Wasserlassen) . In diesem Fall ist es ohne weitere urologische Untersuchung schwierig, den Tumor zu diagnostizieren.
Daher sollte bei einem Fortbestehen der Beschwerden auch nach einer Antibiotikabehandlung der Entzündung oder bei wiederholt auftretenden Blasenentzündungen immer ein Urologe bösartige Veränderungen der Blase durch weitere Untersuchungen ausschliessen.
-
Diagnostik
Bei der Anamnese (Erhebung der Krankengeschichte) wird neben den aufgetretenen Symptomen nach möglichen Risikofaktoren gefragt. Kernbestandteil der Laboruntersuchungen ist die genaue Urinuntersuchung, da es bislang keinen Blasenkrebs-spezifischen Tumormarker im Blut gibt.
Im Urinsediment wird der Urin auf Urinzylinder, Epithelzellen, Leukozyten, Erythrozyten, Bakterien und Kristalle untersucht, wobei nach einer Mikrohaematurie gefahndet wird. Ein zusätzlicher Urin-Streifentest kann die Mikrohaematurie bestätigen.
Urin-Tumormarker (NMP-22, UBC-rapid, BTA)
können Krebszellen im Urin nachweisen, sind allerdings auf Grund ihrer Sensitivität (Vermeiden falsch-negativer Befunde) und Spezifität (Vermeiden falsch-positiver Befunde) nur als ergänzende Urindiagnostik vor einer Cystoskopie (Blasenspiegelung) zu sehen.
In der Urinzytologie wird der Urin auf das Vorliegen krankhafter (pathologischer) Zellen hin untersucht. Auf Grund der hohen Spezifität (Treffsicherheit) von > 90% in der Diagnostik von besonders aggressiven high grade und carcinoma in situ Tumoren sollte in einem dafür spezialisierten zytologischen Labor eine Urinzytologie bei Verdacht auf diese Tumore erfolgen.Mikrohämaturie
Unter Mikrohämaturie versteht man Blutbeimengungen im Urin, die nur unter dem Mikroskop und/oder im Urin-Streifentest nachweisbar sind. Die Leitlinie der amerikanischen Gesellschaft für Urologie (AUA) von 2012 empfiehlt, dass bei Patienten mit wiederholt auftretender, asymptomatischer Mikrohämaturie ohne benigne Ursache eine urologische Diagnostik durchgeführt werden soll.
Bei Verdacht auf einen Blasentumor nimmt der Urologe eine Cystoskopie (Blasenspiegelung), die in aller Regel in Lokalanaesthesie erfolgt , vor, um den Befund zu sichern. Zur Verbesserung der Diagnostik und Therapie des Blasenkarzinoms hat sich in den letzten Jahren in vielen Kliniken und hochspezialisierten Praxen die Fluoreszenzcystoskopie etabliert. In unserer Praxis ist sie bereits seit 1999 Standard (Neue Diagnostik beim Blasenkarzinom).
Zur pathologischen Diagnosesicherung erfolgt das sog. Blasenmapping (Gewebeprobeentnahme aus der Harnblase) und bei gleichzeitiger Therapie die transurethrale Resektion (TURB). Dabei werden alle sichtbaren Tumore mit der Elektroschlinge entfernt. Frühstadien des Blasenkarzinoms, einschließlich des carcinoma in situ, sind bei dem derzeitigen Standardverfahren (Cystoskopie mit Weißlicht) oft nur schwer zu entdecken, weil sie ähnlich wie entzündliche Veränderungen der Blasenschleimhaut aussehen. Um die hohe Rezidivrate (Rückfallquote) von bis zu 70% im ersten Jahr nach TURB zu senken, wird der Eingriff oftmals unter Fluoreszenz-Diagnostik (PDD) durchgeführt.
Man entnimmt daher von allen verdächtig erscheinenden Arealen Gewebsproben. Doch können bei diesem Vorgehen Anfangsstadien von Blasenkrebs übersehen werden, so dass nach kurzer Zeit (3-12 Monate) eine hohe Rückfallquote (Rezidivrate) von 50 bis 70 Prozent beobachtet wird.
Mit der Sonographie (Ultraschalluntersuchung) können Tumore > 3mm in der Harnblase bei einem Füllvolumen > 150 ml erkannt werden. Liegt sonographisch eine Harnstauung der Nieren vor, kann der Urinabfluß aus den Nieren durch weitere Tumore der Harnleiter ( in 5 % der Fälle) verzögert oder blockiert sein.
Zur weiteren Abklärung der Nieren und Harnleiter ist dann ein Infusionsurorgramm (Röntgenuntersuchung der Nieren mit Kontrastmittel ) zusätzlich erforderlich. Bei lokal ausgedehnten Blasentumoren sollte zusätzlich eine Computer- (CT) oder Magnetresonanztomografie (MRT) sowie eine Skelettszintigraphie erfolgen, um das Ausmaß einer möglichen Metastasierung vor der Therapie zu erfassen.
Cystoskopie (Blasenspiegelung )
Die wichtigste Untersuchungsmethode zur Diagnose eines Blasentumors ist die Cystoskopie (Blasenspiegelung). Hier wird nach Einführen eines starren oder flexiblen Cystoskopes über die Harnröhre endoskopisch von innen die Blasenwand untersucht und an einem Videomonitor beurteilt.
Die Cystoskopie kann insbesondere für Männer aufgrund der längeren Harnröhre gegenüber der Frau etwas unangenehm sein, wobei bei vorliegenden entzündlichen Veränderungen im Einzelfall auch vorübergehende Schmerzen nach der Untersuchung auftreten können.
Die Cystoskopie wird in unserer Praxis bei Männern immer mit einem flexiblen (elastischen), sehr dünnen Endoskop durchgeführt, damit die männliche Harnröhre geschont werden kann und somit die Untersuchung für den Mann noch verträglicher ist.
-
Therapie
TUR Blase
Bei der TUR Blase ( Transurethrale Resektion der Blase) wird wie bei einer Blasenspiegelung das Endoskop in die Harnblase über die Harnröhre eingeführt und mit einer ausfahrbaren elektrischen Schlinge das Tumorgewebe aus der Blasenwand vollständig entfernt und zur histopathologischen Untersuchung eingesandt. Der meist etwa 30 minütige Eingriff erfolgt in Narkose, meist als sehr schonende Lumbalanaesthesie (Rückenmarks-nahe Teilnarkose). Nach der Operation wird die Harnblase 1-2 Tage je nach Befund über einen transurethralen Katheter (Harnröhrenkatheter) gespült.
Hybrid-Knife-Verfahren
Größere Blasentumore werden beim Hybrid-Knife-Verfahren in toto (als Ganzes) endoskopisch aus der Blase operiert, so dass eine mögliche Tumoraussaat verhindert werden kann und das entnommene Tumorgewebe durch den Pathologen besser beurteilt werden kann. Das neue OP-Verfahren wird momentan unter Studienbedingungen im Blasentumorzentrum der LMU, mit dem unsere Praxis zusammenarbeitet, durchgeführt.
Das weitere therapeutische Vorgehen hängt von der Beurteilung des Tumorgewebes durch den Pathologen ab, der die Tiefenausdehnung des Blasentumors und dessen Aggressivität beurteilt.
Risiko-adaptierte weitere Therapie beim Blasentumor:
Die Prognose eines Tumors hängt nun von dem Tumorgrading ( Tumoraggressivität, G-Stadium), von dem Tumorstaging ( lokale Tiefenausdehnung, T-Stadium) sowie von einer möglichen Metastasierung des Tumors ( M-Stadium) ab.
Das hierzu verwendete System wird als TNM-Klassifikation bezeichnet.
TNM-Klassifikation (WHO-Klassifikation 2/2016 aktualisiert)
T/pT Primärtumor T0 Kein Anhalt für einen Primärtumor Tis carcinoma in situ: kein infiltrativer/exophytischer (flacher) Tumor Ta exophytisch, nicht infiltrativ Tumor T1 TumorInvasion in die Lamina propria T2 Tumor infiltriert die Muskulatur T2a Tumor infiltriert die oberflächliche Muskulatur (innere Hälfte) T2b Tumor infiltriert die tiefe Muskulatur (äußere Hälfte) T3 Tumor infiltriert perivesikales (ausserhalb der Blase gelegenes) Gewebe T3a Mikroskopisch nachweisbar T3b Makroskopisch nachweisbar T4 Invasion in Nachbarorgane T4a Invasion in die Prostata, Uterus, Vagina T4b Invasion in die Bauch- oder Beckenwand Tx Infiltration nicht beurteilbar N Regionäre Lymphknoten Nx Regionäre Lymphknoten nicht beurteiltbar N0 Kein Anhalt für regionäre Lymphknoten N1 solitäre Lymphknoten-Metastasen (hypogastrisch, obturatorisch, externe iliakale oder präsakrale Lymphknoten) N2 multiple Lymphknoten-Metastasen (hypogastrisch, obturatorisch, externe iliakale oder präsakrale Lymphknoten) N3 Lymphknoten-Metastasen entlang der Aa. iliacae communes M Fernmetastasen Mx Fernmetastasen nicht beurteilbar M0 keine Fernmetastasen M1 Fernmetastasen Risikogruppen des nicht-muskelinvasiven Blasentumors ( aus S3-Leitlinie 2016)
Risikogruppe Tumorstadien Low-risk NMIBC (niedriges Risiko) • solitär pTa,G1 <3cm • solitär pTa,G2 (low grade) <3cm
• PUNLMP (papillary urothelial neoplasm of low malignant potential)
Intermediate-risk NMIBC (mittleres Risiko) • solitär pTa,G1 ≥3cm • multifokal pTa,G1
• solitär pTa,G2 (low grade) ≥3cm
• multifokal pTaG2 (low grade)
• pTa,G2 (high grade)
• Jeder pTa,G2 (wenn keine genaueres Grading bekannt ist)
• Jedes Karzinom aus der Low-risk-Gruppe, das innerhalb von 12 Monaten rezidiviert
High-risk NMIBC (hohes Risiko) Alle Karzinome mit folgenden Kriterien: • pTa,G3
• pT1,G2
• pT1,G3 (high grade)
• pTis (Cis)
• Aggressive histologische Varianten des Urothelkarzinoms mit lymphoepithelialer, plasmazytoider, plattenepithelialer, mikropapillärer und / oder kleinzelliger Komponente sowie nested Variante
Therapie beim nicht-muskelinvasiven Blasentumor (NIMBC)
Ca. 70-80% der Blasentumore sind oberflächlich wachsend, d.h. auf die Schleimhaut der Blase beschränkt (Ta,Cis,T1), ohne dass sie die tieferen Muskelschichten (Ta,Cis,T1) infiltrieren.
Bei diesen nicht-muskelinvasiven , weniger aggressiven (low grade) Tumoren steht die hohe Rezidivrate ( 50-70% innerhalb der ersten 2 Jahre nach Primärdiagnose) im Vordergrund. Die krankheitsspezifische Mortalität ( Risiko an dieser Form von Blasenkrebs zu versterben) ist im Vergleich zu den muskelinvasiven Blasentumoren (T2-T4) gering.
Therapie beim low-risk NIMBC
Die Primärtherapie der low-risk NMIBC ist die vollständige Tumorresektion mittels TUR Blase. Eine Frühinstillation eines Chemotherapeutikums ( z.B. Mitomycin C, Epirubicin, Doxorubicin, Adriablastin) am OP-Ende kann die spätere Rezidivrate senken.
Eine engmaschige urologische Tumornachsorge mit 3-monatigen Cystoskopien (Blasenspiegelungen), Ultraschallkontrollen und Urinuntersuchungen sollte eingehalten werden.
Therapie beim intermediate-risk NIMBC
Die Primärtherapie der intermediate-risk NMIBC ist die vollständige Tumorresektion mittels TUR Blase, gefolgt von einer kurzfristigen erneuten TUR Blase (second look-Operation) nach 4-6 Wochen, bei der der Tumorgrund und –rand auf verbliebene Tumorreste kontrolliert werden.
Die Sekundärtherapie bei stärkerer Tumorausdehnung oder chron. und schnell rezidivierenden (wiederkehrenden) Tumoren besteht in einer adjuvanten (ergänzenden) lokalen Chemotherapie mit einem Chemotherapeutikum (z.B. Mitomycin C, Adriablastin, Epirubicin, Doxorubicin) oder mit BCG bei einer lokalen BCG-Immuntherapie. Nach einem vorgegebenen Therapieschema wird dabei unter ambulanten Bedingungen in unserer Praxis über einen Katheter das Chemotherapeutikum oder das BCG in die Harnblase instilliert. Nach einem Induktionszyklus von 6 Wochen sollte die Therapie über 3 Jahre fortgeführt werden.
Dadurch soll die spätere Rezidivrate (die Wahrscheinlichkeit eines Wiederauftretens des Tumors) verringert werden (Instillationsprophylaxe).
Die engmaschige Tumornachsorge mit 3-monatigen Cystoskopien (Blasenspiegelungen), Ultraschallkontrollen und Urinuntersuchungen und je nach Risikoprofil ergänzende Untersuchungen (Urincytologie, Urin-Tumormarker, Röntgen: CT, MRT, Infusionsurogramm) schließen sich an.
Therapie beim high-risk NIMBC
Die Primärtherapie der high-risk NMIBC ist die vollständige Tumorresektion mittels TUR Blase, gefolgt von einer kurzfristigen erneuten TUR Blase (second look-Operation) nach 4-6 Wochen, bei der der Tumorgrund und –rand auf verbliebene Tumorreste kontrolliert werden.
Die Sekundärtherapie besteht immer in einer adjuvanten (ergänzenden) lokalen BCG-Immuntherapie. Nach einem vorgegebenen Therapieschema wird dabei BCG unter ambulanten Bedingungen in unserer Praxis über einen Katheter in die Harnblase instilliert.
Dadurch soll die spätere Rezidivrate (die Wahrscheinlichkeit eines Wiederauftretens des Tumors) verringert werden (Instillationsprophylaxe).
Die engmaschige Tumornachsorge mit 3-monatigen Cystoskopien (Blasenspiegelungen), Ultraschallkontrollen und Urinuntersuchungen und je nach Risikoprofil ergänzende Untersuchungen (Urincytologie, Urin-Tumormarker, Röntgen: CT, MRT,Infusionsurogramm) schließen sich an.
Therapie beim Therapie-resistenten high-risk NIMBC
Versagt bei einem high-risk NIMBC die Sekundärtherapie mit der adjuvanten (ergänzenden) lokalen BCG-Immuntherapie , erfolgt die weitere Therapie wie bei einem muskelinvasiven Tumor, da eine radikale Cystektomie indiziert ist.
Therapie beim muskelinvasiven Blasentumor Therapie-resistenten NIMBC
Wird bei einer TUR Blase erkannt, dass der Tumor in die Blasenwand hineinwächst und somit eine komplette Entfernung des Tumors endoskopisch nicht möglich ist und/oder in den bildgebenden Verfahren – CT, MRT des Abdomens (Bauchraum) und Thorax (Lungenbereich) mit Kontrastmitteldarstellung- ein fortgeschrittenes Tumorstadium mit Metastasen (z.B. Leber, Lunge, Knochen, Lymphknoten) festgestellt wird, kann eine Heilung derzeit nur durch eine radikale Cystektomie (komplette operative Entfernung der Harnblase) in Aussicht gestellt werden. Dabei werden neben der Blase beim Mann Prostata, Samenblasen, eventuell auch die Harnröhre und die Beckenlymphknoten, bei der Frau Gebärmutter, Eierstöcke, Harnröhre, vordere Scheidenwand und die Beckenlymphknoten entfernt.
Die spätere Harnableitung erfolgt dann über ein ausgeschaltetes Darmteil (Conduit, Pouch) oder über eine aus dem Darm operativ neu-modellierte Blase (Neoblase). Sie erfolgt entweder nicht-kontinent über ein Stoma (Conduit) oder kontinent über eine Neoblase oder katheterisierbaren Pouch.
Eine Neoblase ( Ersatzblase aus Darm) kommt in Bezug auf die Speicher- und Entleerungsfunktion der ursprünglichen Blase am nächsten und wird in >50% als Harnableitung angewandt. Nach Entfernung der Harnblase wird die Ersatzblase an die Stelle der ursprünglichen Harnblase gesetzt und mit den beiden Harnleitern und mit der Harnröhre verbunden, so dass das Wasserlassen über die Harnröhre erfolgen kann.
Nur bei einem Tumorbefall der Harnröhre oder bei entzündlichen Darmerkrankungen kann keine Neoblase als Harnableitung angeboten werden.
Bei einem Ileumconduit wird ein ca. 12-15 cm langes Dünndarmstück ausgeschaltet und in diesen die beiden Harnleiter eingepflanzt. Das nach außen gewandte Ende des Conduits wird im Unterbauch durch die Haut ausgeleitet, so dass über ein Beutelsystem, das auf die Haut geklebt wird, der Urin gesammelt und vom Patienten regelmäßig geleert und gewechselt werden kann.
Der durchtrennte Darmanteil wird wieder zusammengenäht und dient weiterhin der Stuhlpassage. Die Operation ist seit über 50 Jahren etabliert und wird vor allem bei älteren Patienten durchgeführt, bei denen ein weit fortgeschrittener Tumor vorliegt oder eine simultane Urethrektomie (Entfernung der Harnröhre) bei Tumorbefall der Harnröhre notwendig ist.
Alternativ zum Ileumconduit kann ein aus Darmteilen modelliertes Urin-Reservoir, das über ein dicht schließendes Stoma im Unterbauch oder im Bauchnabel mündet, gebildet werden. Der Pouch wird vom Patienten mit einem Katheter regelmäßig entleert. Diese Form der Harnableitung kommt gerade für Patienten in Frage, bei denen der Wunsch nach einem kontinenten Stoma besteht (katheterisierbarer (kontinenter) Pouch).
Chemotherapie beim Blasentumor
Eine Chemotherapie wird immer dann notwendig, wenn Metastasen (Tumorabsiedlungen) vor oder auch nach einer radikalen Operation der Harnblase nachweisbar sind. Hierbei handelt es sich um eine Polychemotherapie, bei der verschiedene Chemotherapeutika kombiniert in einer bestimmten Reihenfolge und Dosierung verabreicht werden. Die Chemotherapeutika greifen die sich sehr schnell teilenden Zellen (Tumorzellen, aber auch Darmzellen, Haarzellen, Blutzellen) an und können die Tumorzellen zerstören, aber auch stärkere Nebenwirkungen hervorrufen. Heute wird eine Kombination aus Cisplatin und Gemcitabine verwendet, die das frühere Therapieschema mit MVEC und MVAC ersetzt und deutlich verträglicher ist. Somit ist in den meisten Fällen eine ambulante Chemotherapie möglich.
Neoadjuvante Chemotherapie beim muskelinvasiven Blasentumor
Die neoadjuvante Chemotherapie erfolgt bei einem muskelinvasiven Blasentumor unabhängig vom Lymphknotenstatus vor einer radikalen Cystektomie.
Insgesamt führt eine neoadjuvante Chemotherapie zu einer Reduktion der Gesamtmortalität von 14% nach 6,4 Jahren. Es gibt keine bevorzugte Kombination von Chemotherapeutika und es sollten 3-4 Zyklen gegeben werden. Nur für Kombinationstherapien mit Cisplatin gibt es belastbare Daten bei Patienten mit guter Nierenfunktion und mit gutem Allgemeinzustand .
Adjuvante Chemotherapie beim muskelinvasiven Blasentumor
Die adjuvante Chemotherapie erfolgt bei organüberschreitenden (>pT3) Blasentumoren und unabhängig vom Tumorstadium bei Lymphknotenmetastasen des Blasentumors (pN1) nach einer radikalen Cystektomie.
Insgesamt führt eine adjuvante Chemotherapie zu einer moderaten Reduktion der Gesamtmortalität. Es gibt keine bevorzugte Kombination von Chemotherapeutika und die Zahl der Zyklen ist nicht festgelegt. Wichtig ist hingegen eine Kombination mit Cisplatin, so dass für eine adjuvante Chemotherapie nur Patienten mit guter Nierenfunktion und mit gutem Allgemeinzustand in Frage kommen.
-
Tumornachsorge
Nachsorge des nicht-muskelinvasiven Blasentumors
Das nicht-muskelinvasive Blasenkarzinom (NIMBC) hat zwar eine deutlich geringere krankheitsspezifische Mortalität (Sterberisiko) verglichen mit den muskelinvasiven Harnblasenkarzinomen (T2-4) , aber hohes Rezidiv- und Progressionsrisiko , so dass eine regelmäßige Tumornachsorge beim Urologen erfolgen muß.
In unserer Praxis werden alle notwendigen Tumornachsorge-Untersuchungen evidenz-basiert nach der akutellen S3-Leitlinie für Blasentumore in Abhängigkeit vom Risikoprofil des NMIBC durchgeführt.
Nachsorge von muskelinvasiven/metastasierten Blasentumoren nach Cystektomie/ Chemotherapie
Die Tumornachsorge der fortgeschrittenen Blasentumore, die radikal operiert und ggfs. auch chemotherapiert worden sind, dient dem frühzeitigen Rezidiv- bzw. Metastasennachweis, um eine weitere Tumortherapie einzuleiten. Hierbei werden auch funktionelle Störungen der Nieren und der Harnableitung erfasst.
In unserer Praxis werden alle notwendigen Tumornachsorge-Untersuchungen evidenz-basiert nach der akutellen S3-Leitlinie für Blasentumore durchgeführt.
Die radiologische Zusammenarbeit für die weiterführende Bildgebung (z.B. CT , MRT, Nierenfunktionsüberprüfung, Skelettszintigraphie) erfolgt mit der Radiologie Starnberger See.
Die onkologische Zusammenarbeit erfolgt mit den onkologischen Praxen im Landkreis Starnberg www.onkologie-starnberg.de, www.onkologie-herrsching.de und mit dem Blasentumorzentrum der LMU in der Urologischen Klinik und Poliklinik München-Großhadern
-
Neue Diagnostische Methoden beim Blasenkarzinom
Bei der Cystoskopie (Blasenspiegelung) können Vorstufen von Blasentumoren oder auch sehr winzige Blasentumore nicht immer zuverlässig erkannt werden.
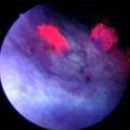
Um die Harnblasentumoren besser und frühzeitiger zu entdecken, wurde die Photodynamische Diagnostik (PDD), bei der ein Fluoreszenzfarbstoff (Hexalaevulinsäure) die Harnblasentumorzellen anfärbt, entwickelt.
Der Fluoreszenzfarbstoff wird vor der Cystoskopie (Blasenspiegelung) über einen Katheter in die Blase eingegeben und verbleibt für mindestens 1h in der Blase .
Dort bindet sich der Farbstoff spezifisch an die Tumorzellen oder Dysplasien (Tumorvorstufen). Unter fluoreszierendem violetten Licht mit einer Wellenlänge von ca. 400nm, werden die ansonsten schlecht erkennbaren Tumorareale durch die typische Rotfluoreszenz sichtbar, während umliegendes normales Harnblasengewebe weiterhin violett erscheint. Dadurch kann das Tumorgewebe eindeutig und leicht vom gesunden Gewebe der Harnblase unterschieden werden. Die Überlegenheit der Fluoreszenz-Cystoskopie (PDD) gegenüber der bislang eingesetzten Cystoskopie mit Weisslicht zeigt sich auch dadurch, dass bis zu 20% mehr Harnblasenkarzinome und deren Vorläuferstadien entdeckt werden.
Leicht können auch bei der primären endoskopischen Operation der Harnblase (TUR Blase ) Tumore aufgrund ihres flachen Wachstums (Carcinoma in situ) oder ihrer geringen Größe übersehen werden. Hierbei kann die PDD-gesteuerte Operation eine größtmögliche Sicherheit geben, dass der nicht-muskelinvasive Harnblasentumor vollständig entfernt wird. Wissenschaftliche Studien konnten zeigen, dass mit Hilfe der PDD vermehrt Tumore gefunden werden können und somit die Wahrscheinlichkeit eines Wiederkehrens des Tumors gesenkt werden kann.
Die Rate an Frührezidiven der oberflächlichen Tumore wird damit gesenkt, was ein besserer prognostischer Faktor für den Verlauf der Erkrankung bedeutet.
Seit 1999 setzen wir in unserer Praxis und in der Urologischen Klinik Starnberg die Photodynamische Diagnostik (PDD) bei der Endoskopie und bei endoskopischen Operationen der Harnblase (TUR, Laser) ein.
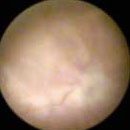
Beispiel 1:
Nachweis einer aggressiven Blasenkrebsvorstufe (Carcinoma in situ)Unter Weißlicht
Unter Fluoreszenzlicht (PDD)
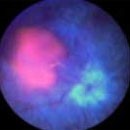
Beispiel 2:
Nachweis eines oberflächlich wachsenden BlasentumoresUnter Weißlicht
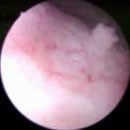
Unter Fluoreszenzlicht (PDD)